INTRODUCTION
La mucoviscidose est une maladie génétique rare qui se caractérise par un dysfonctionnement de la sécrétion du mucus, qui est plus visqueux et plus abondant. Elle peut toucher plusieurs organes, principalement les voies respiratoires, mais aussi les systèmes digestif et reproductif. Sur le plan pulmonaire, l’encombrement des bronches rend les patients plus sensibles aux infections bactériennes. Les symptômes de la maladie se traduisent alors par une toux chronique, puis par l’inflammation des voies aériennes qui, devenant répétitive, s’accompagne d’une détérioration progressive des tissus pulmonaires et une perte parfois très importante de la capacité respiratoire. Les patients les plus gravement touchés souffrent d’une insuffisance respiratoire pouvant nécessiter une greffe pulmonaire et mener, à terme, à leur décès. L’anticipation de ces exacerbations représente ainsi un point d’ancrage essentiel dans l’expérience de la mucoviscidose. À cet égard, les modalités de suivi et les formes de surveillance mises en place jouent un rôle central dans l’amélioration de la qualité de vie des patients (Bell et al., 2020). C’est ce dont témoignent les évolutions de la prise en charge depuis le début des années 2000, avec la généralisation du dépistage néonatal systématique, qui permet d’effectuer un diagnostic précoce, et la création de centres de ressources et de compétences de la mucoviscidose (CRCM) qui suivent les patients dans le cadre d’une prise en charge pluridisciplinaire (Travert et al., 2024). Ces deux avancées ont permis d’améliorer grandement la qualité et l’espérance de vie des personnes touchées par cette maladie.
Dans cet article, nous proposons d’analyser les modalités d’introduction d’un dispositif d’autosurveillance numérique dans le quotidien des patients atteints de mucoviscidose, pour aider ces derniers à mieux anticiper les exacerbations de la maladie, de manière plus autonome, en dehors du milieu médical. Ce dispositif se compose d’un ensemble d’objets connectés (montre, balance, sous-matelas et spiromètre) qui permettent de relever et de suivre des paramètres physiologiques (oxygénation, fréquence cardiaque, cycles de sommeil, poids, nombre de pas, etc.) au sein d’une application mobile où le patient peut également saisir des informations manuellement (ressentis corporels ou traitements). Il est conçu par un jeune patient dans le cadre de son projet de fin d’études en école d’informatique, d’après l’idée forgée au cours de sa propre expérience, selon laquelle la quantification de ces paramètres, ainsi que la visualisation conjointe de leur évolution apportent une information nouvelle permettant d’anticiper une dégradation de l’état de santé, voire de prévenir celle-ci en ajustant son comportement. L’objectif est ainsi de construire un support de connaissance de soi, concernant son corps, ses activités quotidiennes et sa maladie, et de contribuer à l’éducation thérapeutique du patient qui, ce faisant, peut acquérir plus d’autonomie dans la gestion de sa pathologie.
Comment s’élaborent les usages du dispositif d’autosurveillance par les patients ? De quelles façons ces usages font-ils évoluer l’expérience et la prise en charge de la mucoviscidose ? Dans quelle mesure ce dispositif favorise-t-il l’autonomisation des personnes atteintes, tant recherchée par les différents intervenants de la relation de soin ? Nous proposons d’aborder ces questions à partir d’une recherche longitudinale réalisée entre 2020 et 2022[1], auprès de 13 patients invités par leur équipe soignante à essayer une première version du dispositif à leur domicile pendant une durée de 6 mois, selon la fréquence et les modalités de leur choix[2]. L’étude repose sur des entretiens semi-directifs approfondis (n=37) auprès des patients, qui ont été interrogés trois fois à 6 mois d’intervalle. Elle se fonde aussi sur des entretiens avec des professionnels de santé exerçant en milieu hospitalier (n=8) ou en cabinet libéral (n=20), dont la perspective est mobilisée ici de façon plus secondaire. Si l’objectif initial était de connaître la manière dont le dispositif vient équiper le patient pour soutenir son autonomisation, cette recherche a été réalisée dans un contexte de soin bouleversé par l’arrivée d’un nouveau traitement médicamenteux hautement efficace, le Kaftrio®, qui a été mis sur le marché en 2021 par le laboratoire Vertex. Cette trithérapie s’est en effet accompagnée d’une amélioration très rapide et remarquable de l’état de santé d’un grand nombre de patients, pouvant aller jusqu’à la disparition de certains symptômes, permettant à la fois de diminuer les risques d’exacerbation et d’alléger les soins quotidiens. Les questions liées à l’autonomisation des patients se voient ainsi reformulées avec la recomposition de l’expérience de la mucoviscidose, qui devient une maladie chronique avec laquelle les patients doivent apprendre à vivre plus longtemps, dans le cours d’une trajectoire désormais reconfigurée par un nouvel horizon du possible. Dans ce contexte thérapeutique, les usages du dispositif d’autosurveillance numérique se sont développés suivant des modalités qui n’étaient pas prévues initialement, ni par les concepteurs ni par les soignants.
Nous présenterons tout d’abord les spécificités et les enjeux de la surveillance de la mucoviscidose, qui repose sur des efforts particulièrement importants de la part des patients dont la coopération et la participation aux soins, bien qu’attendues par les soignants, demeurent souvent invisibles et peu reconnues dans l’organisation du travail médical (Star, 1991 ; Star & Strauss, 1999 ; Strauss, 1985). L’analyse met ainsi en évidence la manière dont le « travail du patient » (Strauss et al., 1982) atteint de mucoviscidose, en particulier les tâches liées à la surveillance de la maladie qui visent à autonomiser les patients, font régulièrement l’objet de négociations entre les différents protagonistes de la relation de soin (Baszanger, 1986). L’article présente ensuite les modalités d’appropriation du dispositif d’autosurveillance numérique par les patients, ainsi que leurs logiques de quantification qui, dans le contexte d’une amélioration de l’état de santé avec le Kaftrio, se rapprochent des pratiques usuelles de Quantified Self (Dagiral et al., 2019 ; Lupton, 2016a). En conclusion, nous verrons que si le travail du patient évolue effectivement avec l’intégration des objets connectés dans la vie courante, leur utilisation dans ce contexte particulier est davantage liée au « travail sur la vie quotidienne avec la maladie », plutôt qu’au « travail sur la maladie », périmètre initialement visé par les concepteurs du dispositif.
L'EXPÉRIENCE DE LA MUCOVISCIDOSE, LE "TRAVAIL DU PATIENT" ET LES ENJEUX DE L'AUTOSURVEILLANCE NUMÉRIQUE
Comme pour toute maladie chronique, une dimension essentielle de l’expérience de la mucoviscidose réside dans les nombreux efforts que les patients doivent fournir afin d’assurer leur propre prise en charge. Il existe cependant très peu de recherches permettant de rendre compte de l’expérience de cette pathologie, c’est-à-dire de la façon dont le patient « vit » sa maladie, subjectivement, suivant ses perceptions sensorielles et ses ressentis corporels, les émotions et les sensations qu’il éprouve, ainsi que les raisonnements et les logiques d’action qu’il développe, à la fois dans le soin et dans la vie quotidienne (Ferez et al., 2023; Pichonnaz, 2024). En effet, les travaux s’intéressent davantage au travail des professionnels de santé et à la prise en charge hospitalière où le patient joue un rôle plus limité, par exemple dans le cadre de l’éducation thérapeutique (Frattini et al., 2009; Langeard et al., 2011; Langeard & Minguet, 2018; Rault et al., 2015, 2015). L’expérience de la mucoviscidose, quant à elle, est abordée souvent à travers la notion de « qualité de vie » et, dans nombre de cas, son approche traite avant tout de la souffrance physique et psychique qui jalonne la trajectoire des patients (Jamieson et al., 2014; Raveneau, 2020). De ce point de vue, la mucoviscidose présente des caractéristiques communes avec d’autres maladies chroniques comme le diabète ou le cancer (Baszanger, 1986 ; Bury, 1982 ; May et al., 2014) : relation thérapeutique au long cours, aggravation des symptômes et fardeau du traitement, pratiques de mesure et de suivi des paramètres physiologiques, ajustements successifs des narrations biographiques, etc. Néanmoins, la mucoviscidose renvoie aussi à un ensemble de particularités dont il importe de rendre compte afin de mieux saisir l’expérience subjective des patients, ainsi que les enjeux du travail de surveillance dans la prise en charge.
La mucoviscidose, une expérience de maladie chronique singulière
Une des particularités les plus importantes de la mucoviscidose réside dans le profil des personnes atteintes, qui deviennent des patients dès leur plus jeune âge et qui développent, avec le temps, une connaissance relativement poussée de leur maladie. Cet apprentissage se fait de différentes manières, au sein du foyer familial où parfois plusieurs membres sont touchés par la maladie. Il s’effectue aussi au sein du milieu hospitalier, aux côtés des professionnels de santé, dans divers contextes d’éducation thérapeutique (ETP) qui peuvent être plus ou moins formalisés (David et al., 2007). Il est enfin assuré par divers collectifs (associations de patients, sociétés savantes, etc.) constitués autour de la pathologie, ainsi que lors des échanges avec d’autres patients atteints de mucoviscidose, par exemple au sein de groupes de parole ou d’espaces numériques de discussion. L’apprentissage constitue un travail continu pour ces patients dont certains distinguent clairement la connaissance théorique générale de la maladie et la dimension singulière, personnelle et tacite des savoirs sensoriels et expérientiels acquis empiriquement, qui sont difficiles à partager :
« […] une bonne partie, c’était pas tant de connaître la maladie, mais connaître ma maladie. Ce qui est différent des fois […] Ma maladie, je la connais très bien, excellemment bien, j’ai envie de dire. "La" maladie, peut-être moins. » (Pierre, 25-30 ans, forme stable de la maladie, sous Kaftrio)
Comparativement à d’autres pathologies chroniques, la mucoviscidose se caractérise en effet par la très grande variabilité de ses manifestations, les symptômes et l’expérience subjective pouvant être très différents d’un patient à l’autre. Les enquêtés témoignent ainsi, pour une large part, d’une très bonne connaissance de « leur » maladie, c’est-à-dire de ses manifestations spécifiques dans leur cas particulier. Touchant plusieurs organes, la pathologie s’accompagne également de diverses comorbidités qui participent à la singularisation de cette expérience : les patients cumulent souvent plusieurs maladies chroniques, dont le diabète est la plus commune. La singularité des cas s’accentue davantage avec la rareté des mutations génétiques associées à la mucoviscidose qui, de manière générale, est peu connue dans le monde médical, et encore moins au-delà de celui-ci.
Une autre particularité de l’expérience de la mucoviscidose réside dans la manière dont sa prise en charge est organisée, à travers un suivi longitudinal et pluridisciplinaire, au sein de CRCM spécialisés d’abord en pédiatrie, puis dans le suivi des patients adultes. Prendre en charge les patients atteints de mucoviscidose requiert des connaissances médicales pointues et pluridisciplinaires, touchant à diverses spécialités. Selon la typologie et la sévérité de leur pathologie, les patients sont suivis par de nombreux professionnels de santé (kinésithérapeute, gastroentérologue, diabétologue, endocrinologue, gynécologue, psychologue, ORL, pharmacien, infirmier, etc.) dont certains les connaissent depuis leur plus jeune âge. Parmi les praticiens, les pneumologues jouent un rôle particulier. La mucoviscidose touchant principalement les poumons, ces spécialistes sont en effet désignés comme médecins référents des patients dont ils participent à coordonner les soins. Pour de nombreux patients, le pneumologue est aussi consulté pour des questions de santé sans lien direct avec la mucoviscidose ou les voies respiratoires :
« […] il y a des consultations, on parle autant de douleur abdominale que de crachat, en fait. Cela nécessite qu’on soit un peu plus polyvalents. Enfin, ça fait partie du spectre de la mucoviscidose, donc on connaît… » (Dr Nicole, pneumologue junior, CRCM)
Si les activités réalisées par les soignants s’organisent autour des signes cliniques de la maladie, à travers des préconisations désormais standardisées (Kerem et al., 2005), elles varient aussi selon des aspects non médicaux, liés notamment à la façon dont les patients vivent avec leur pathologie (problèmes sociaux, scolarité, parentalité, etc.). La prise en charge de la mucoviscidose est ainsi caractérisée par une relation thérapeutique particulière, où le suivi s’organise non seulement au long cours, mais aussi à travers une très forte proximité avec l’équipe soignante. Cette proximité sociale, essentielle pour établir une relation thérapeutique efficace, se constitue au fil du temps, à travers un processus de négociation qui porte sur l’organisation du travail de prise en charge de la maladie au sein d’un réseau d’acteurs et de lieux hétérogènes.
Le « travail du patient » atteint de mucoviscidose : des efforts particulièrement importants
La notion du « travail du patient » est utilisée originellement dans le contexte des maladies chroniques dont la prise en charge est caractérisée, entre autres, par la complexification des technologies médicales qui l’accompagnent (Mathieu-Fritz & Guillot, 2017; Strauss et al., 1981; Trupia et al., 2021). Elle vise à décrire les différentes formes de travail que le patient doit réaliser à la fois lors d’un séjour à l’hôpital (Strauss et al., 1982), et en dehors de celui-ci, dans la vie quotidienne (Corbin & Strauss, 1985). Cette notion permet de décrire avec justesse l’expérience de la mucoviscidose qui se caractérise par les efforts conséquents auxquels le patient doit consentir, à la fois au sein du milieu médical, en acceptant notamment le suivi et les soins proposés par les professionnels de santé, et dans le cadre des espaces domestiques et familiaux, en prenant ses traitements, en respectant les consignes pour minimiser les risques associés à la maladie, ou encore, en surveillant les variations de son état de santé pour prévenir les éventuelles exacerbations.
Le « travail du patient » atteint de mucoviscidose est en effet particulièrement important. Les patients doivent réaliser chaque jour toute une série d’activités et de tâches très diverses, afin de garantir le bon déroulement des soins médicaux. Au-delà des tâches directement liées aux soins, le travail du patient comprend également des activités plus périphériques qui contribuent à ces derniers (Strauss, 1985) : le « travail de machine » qui renvoie à l’appropriation, à la connaissance et à l’entretien des technologies médicales utilisées ; le « travail de sécurité clinique » qui repose sur la surveillance de constantes comme le Volume Expiratoire Maximal par Seconde (VEMS) ; le « travail de confort » qui a pour objectif de soulager une gêne ou une douleur, ainsi que le « travail d’articulation » qui consiste à se coordonner avec les différents protagonistes de la relation de soin, et le « travail d’information » qui vise à produire, interpréter et transmettre des informations liées à la maladie. Par ailleurs, le patient doit aussi faire face aux craintes, aux attentes et aux interrogations qui s’expriment sur le plan émotionnel, affectif et psychologique. De tels efforts renvoient à un « travail sur les sentiments », c’est-à-dire sur la patience ou le sang-froid par exemple, de même qu’au « travail sur l’identité » et au « travail sur la biographie » qui visent à intégrer la maladie, c’est-à-dire son degré de gravité et ses évolutions, à la définition de soi et aux représentations de sa vie future (Bury, 1982). Enfin, le travail du patient va au-delà du « travail sur la maladie » ; il comprend également le « travail sur la vie quotidienne avec la maladie », c’est-à-dire tous les efforts d’anticipation des effets de la pathologie sur les activités quotidiennes et, de façon symétrique, des conséquences de ces activités sur les manifestations de la maladie. Il s’agit par exemple d’anticiper les déplacements qui impliquent de préparer à l’avance les dispositifs médicaux et les médicaments à prendre au cours de la journée. L’anticipation des patients atteints de mucoviscidose est aussi celle des efforts physiques et de la fatigue qu’ils vont susciter, ou encore celle des effets de l’environnement social et matériel sur la maladie (pollution, poussière, humidité, rassemblements humains, etc.). Le patient doit ainsi développer des formes d’attention particulière pour gérer chaque jour sa pathologie et organiser ses activités quotidiennes en intégrant les contraintes qui lui sont propres.
Un exemple particulièrement frappant qui illustre la densité de ce travail, est celui des tâches de soin « directes », qui concernent notamment la prise des traitements. Les patients doivent en effet prendre en moyenne entre 25 à 35 médicaments par jour ; le plus touché par la dimension polypathologique de la maladie comptant jusqu’à 56 médicaments qui doivent être pris à des moments différents de la journée et suivant des conditions variables, parfois à jeun, d’autres fois pendant ou après manger, ou avant de se coucher. Bien entendu, ce nombre peut varier considérablement selon les périodes (cures d’antibiotique, de vitamines, etc.), renvoyant ainsi à la dimension évolutive de cette organisation. Beaucoup de patients recourent à des piluliers qu’ils préparent généralement pour plusieurs jours, voire plusieurs semaines, l’objectif étant de composer avec les contraintes pratiques du quotidien :
« Si je pars, je dois aller partout avec mon pilulier pour être sûre d’avoir tous mes médicaments avec moi. Normalement, ça doit être fait par une infirmière, mais j’ai appris à le faire toute seule et je le fais quasi… généralement, je le fais le dimanche pour une semaine et je le fais chaque semaine. Et je mets mes médicaments matin, midi, soir, et coucher. Donc voilà, j’en ai 4 ». (Lilianne, 30-35 ans, forme grave de la maladie, non éligible au Kaftrio)
Les patients veillent ainsi constamment à gérer leurs stocks de médicaments, qu’ils doivent souvent prévoir bien à l’avance afin de ne jamais en manquer. Cette anticipation est d’autant plus importante pour les médicaments plus rares en pharmacie, qui nécessitent de passer des commandes avant que les stocks du patient ne soient épuisés. Ce travail de coordination qui s’amplifie lors des déplacements de plusieurs jours, voire de plusieurs semaines, peut constituer une véritable épreuve pour un patient peu aguerri. Cela dit, la majorité des patients définissent ce travail d’anticipation comme un automatisme acquis au fil du temps, qui représente finalement le travail le moins intense du spectre des activités à réaliser au quotidien.
Les soins perçus comme les plus exigeants sont en effet ceux qui contraignent les patients à s’extraire de leurs activités quotidiennes. Il s’agit par exemple des exercices de drainage des voies respiratoires qu’ils doivent souvent effectuer avec un kinésithérapeute. Le travail du patient relève alors d’une temporalité particulière marquée par une séquentialité précise des activités, avec notamment la nécessité d’anticiper l’organisation des rendez-vous quotidiens ou pluri-hebdomadaires avec le kinésithérapeute. En amont de chaque séance, les patients doivent parfois utiliser des produits nébulisés permettant de fluidifier leurs bronches pour améliorer l’efficacité des exercices respiratoires. Certains prennent ce type de traitement par aérosol qui nécessite d’être immobilisé pendant une vingtaine de minutes, parfois plusieurs fois par jour. Malgré tous ces efforts, ce travail peut demeurer cependant insuffisant pour certains patients qui doivent recourir à un dispositif d’assistance respiratoire d’oxygénothérapie au moment de l’effort physique ou pendant la nuit.
L’autosurveillance des patients, entre « ordre négocié » et prescriptions contradictoires
Le travail du patient atteint de mucoviscidose se caractérise ainsi par son aspect à la fois très poussé, adaptatif et évolutif. Mais l’importance de ce travail s’observe également à travers sa dimension collective et son inscription au sein d’un réseau d’acteurs nombreux et hétérogènes qui contribuent à surveiller et à soigner les symptômes de la maladie, au sein de lieux très divers. Ce travail s’effectue à la frontière et au sein d’espaces occupés par différents intervenants avec lesquels il est parfois partagé : le patient peut déléguer une partie des activités à réaliser aux proches ou aux soignants qui vont prendre en charge certaines tâches de surveillance et de confort, par exemple au cours d’une hospitalisation. On observe aussi des phénomènes de relais thérapeutiques plus importants mis en place dans le cadre d’un suivi plus régulier, notamment par les kinésithérapeutes. La dimension collective du travail de surveillance et l’intensité des soins caractérisent ainsi cette prise en charge par des formes « d’alliance thérapeutique » spécifiques qui se créent au moyen de négociations régulières visant à se répartir ce travail. En raison du nombre de professionnels qui interviennent, cette prise en charge repose, pour les différents protagonistes, sur la capacité à se coordonner et à s’accorder sur la définition des objectifs thérapeutiques, autour de l’autonomisation des patients. La coordination des soins se construit ici comme un « ordre négocié », à travers des tentatives de persuasion, des arrangements et des compromis qui permettent de se mettre d’accord, le plus souvent de façon informelle, sur la meilleure façon d’organiser cette autonomie au quotidien (Baszanger, 1986; Strauss, 1978, 1992).
Dans le domaine de la santé, l’idée d’autonomie est souvent relayée par la notion fort répandue d’empowerment (ou encapacitation) des patients, qui renvoie à la participation croissante de ces derniers aux processus décisionnels concernant leur santé (Anderson & Funnell, 2010; Castro et al., 2016) et au développement de leur capacité à agir sur la maladie. Pour devenir « capables », les patients doivent notamment acquérir des compétences contribuant à les rendre plus autonomes vis-à-vis des professionnels et des organisations de soin. Mais la prise en charge des pathologies chroniques évolue selon des prescriptions et des incitations qui sont parfois contradictoires : si le point de vue et l’expérience subjective des patients sont davantage pris en compte dans les décisions thérapeutiques, l’emprise sociale de la logique médicale devient également de plus en plus importante dans la vie des patients (Ménoret, 2015). Cette tension est d’autant plus structurante dans l’expérience des personnes atteintes de mucoviscidose, qui doivent apprendre à vivre avec cette pathologie dès leur plus jeune âge. Une situation paradoxale s’installe ainsi dans la relation thérapeutique qui, marquée par une incitation forte à l’autonomisation des patients, se construit à travers une extension importante de la logique médicale au sein de divers domaines de la vie quotidienne (travail, loisirs et relations sociales). C’est ce dont témoigne un soignant qui définit les objectifs thérapeutiques dans les termes d’une élaboration, d’une évaluation et d’un accompagnement dans la mise en place d’un projet de vie :
« [Mon rôle,] c’est accompagner une personne atteinte d’une maladie que je connais […] sur le plan des objectifs très médicaux, physiques et cliniques, mais aussi de suivre cette personne dans ce qui est... de l’aider à avoir la vie de la meilleure qualité possible, la plus normale possible. […] Et c’est probablement presque ce qui nous prend le plus de temps maintenant. […] l’aider à avoir des projets. » (Dr Margot, pneumologue senior, CRCM)
Les soignants véhiculent ainsi une « philosophie autonomiste », concevant le patient comme un sujet de soin, actif, réactif et réflexif, qui non seulement travaille à sa propre prise en charge, mais aussi porte des projets de vie (Mol, 2009). Si les patients sont invités à s’autonomiser, ils doivent cependant le faire à travers des modalités qu’ils négocient avec l’équipe soignante et qui, pour une part, s’imposent à eux. Le caractère paradoxal de la situation émerge au cours de ces négociations. Même si celles-ci portent avant tout sur l’appropriation de la maladie qui ne doit pas être oubliée ou déniée par le patient, elles se prolongent également dans une quête du « juste soin » portée par les soignants : malgré sa pathologie, le patient doit essayer d’avoir la vie la plus normale possible. Il doit atteindre, de façon négociée et co-construite, une forme d’équilibre entre traitement médical et qualité de vie avec la pathologie. Or l’enjeu de la prise en charge ne se définit pas toujours en ces termes pour les patients qui doivent normaliser la maladie, c’est-à-dire prétendre vivre une vie normale, tout en participant activement à la gestion de la pathologie (Carricaburu & Ménoret, 2004; Strauss, 1975). Les définitions du juste soin, ainsi que la capacité à le mettre en œuvre concrètement peuvent évoluer en fonction d’un ensemble d’éléments et d’événements auxquels les patients font face en dehors du milieu hospitalier. L’autonomisation s’effectue non seulement au prix de traitements lourds, contraignants et techniquement exigeants, qui sont désormais intégrés au sein du domicile, mais aussi à travers un travail particulièrement soutenu pour vivre, paradoxalement, comme un non-malade (Bach, 1995; Carricaburu, 2000). Une autre contradiction émerge ici, laissant transparaître le rapport parfois conflictuel à la pathologie dans le cadre duquel le patient doit lutter contre les effets de celle-ci au quotidien, afin d’en réduire la portée. Pour accroître leur autonomie face à la maladie, les patients doivent ainsi consacrer plus de temps à se soigner, et être davantage à l’écoute de leur corps et de leur ressenti. S’ils peuvent dissimuler la maladie aux yeux d’autrui, les patients doivent ainsi développer, a contrario, une attention particulière à ses manifestations pour qu’elle occupe moins de place dans la vie quotidienne.
Au-delà de la sphère familiale, ce travail de surveillance est partagé avec les soignants du CRCM et les professionnels libéraux, qui suivent les signes cliniques dans le cadre des consultations et des séances thérapeutiques. Il s’agit là d’un « travail de sécurité clinique » (Strauss, 1985) qui consiste à contrôler et à évaluer des signes et des indicateurs plus ou moins nombreux et fiables des manifestations de la pathologie. Mais au-delà des principaux « marqueurs » tels que la capacité respiratoire, qui permettent de suivre les symptômes les plus explicites, les risques associés à la maladie nécessitent de développer une surveillance beaucoup plus constante et spécifique pour évaluer l’état de santé global des patients. C’est là sans doute une particularité de la surveillance de la mucoviscidose qui, à la différence d’autres pathologies chroniques, ne renvoie pas à un seul paramètre, mais à plusieurs indicateurs comme le poids ou la fréquence cardiaque au repos, qui sont souvent de nature secondaire par rapport aux atteintes pulmonaires et digestives les plus évidentes, dont l’importance peut varier d’un patient à l’autre. La surveillance des divers paramètres se fait à l’aide d’informations sensorielles « ressenties » (fatigue, douleurs, maux de tête, encombrement, etc.) et « mesurées » (diminution du VEMS, perte de poids, etc.) qui s’articulent souvent dans la durée, et de manière spécifique à chaque patient, pour constituer des repères sensoriels, c’est-à-dire des indicateurs et des seuils d’alerte basés sur des « signaux faibles » permettant d’identifier les prémices des exacerbations. C’est précisément cette forme d’attention et de vigilance que le dispositif d’autosurveillance numérique cherche à équiper, pour aider les patients à mieux anticiper les manifestations de la mucoviscidose.
MODALITÉS D’APPROPRIATION ET LOGIQUES D’USAGES DU NOUVEAU DISPOSITIF D’AUTOSURVEILLANCE NUMÉRIQUE
Comme dans le cas du diabète (Bruni & Rizzi, 2013; Moretti & Morsello, 2017), le dispositif d’autosurveillance numérique vise à améliorer l’efficacité du travail de surveillance. Mais il est proposé dans un contexte de soin profondément bouleversé par l’arrivée du Kaftrio. En produisant une amélioration importante de l’état de santé de la majorité des patients, ce nouveau traitement a contribué à reformuler les enjeux d’autonomisation initialement portés par le dispositif. Si les patients disent trouver celui-ci utile pour suivre certains signes cliniques durant les périodes d’aggravation de leur état de santé, l’intérêt pour l’autosurveillance se voit cependant redéfini dans un contexte où le travail de surveillance est désormais soulagé[3] : quand de nombreux patients arrêtent la kinésithérapie respiratoire pratiquée jusque-là quotidiennement, l’équipe soignante s’interroge de son côté sur la possibilité d’espacer davantage les consultations de suivi des patients dont l’état de santé est désormais stabilisé. Si les améliorations apportées par le nouveau traitement expliquent la relative faiblesse des usages du dispositif que nous avons pu constater au cours de la recherche, l’analyse montre que nombre de patients l’ont tout de même intégré dans leur quotidien, suivant des logiques de quantification sensiblement différentes de celles envisagées initialement. C’est ce que nous proposons d’étudier, en deux temps.
Des difficultés d’appropriation aux modalités multiples d’intégration des objets connectés
Le dispositif d’autosurveillance numérique est constitué par quatre objets connectés (une montre, une balance, un sous-matelas et un spiromètre) qui permettent d’effectuer une série de mesures et de visualiser celles-ci conjointement au sein d’une application mobile. La montre connectée est l’objet qui permet d’enregistrer le plus de paramètres physiologiques : nombre de pas, saturation en oxygène, cycles de sommeil, fréquence cardiaque au repos et lors de différentes activités physiques. La balance connectée informe sur le poids et l’indice de masse corporelle, grâce à une courbe d’évolution. Le capteur de sommeil calcule un score à partir de différentes informations sur la qualité du sommeil, telles que les phases profondes ou légères, les interruptions, les apnées ou encore les ronflements. Le spiromètre mesure le VEMS qui est l’indicateur de référence pour évaluer la capacité pulmonaire des personnes atteintes de mucoviscidose. En centralisant toutes ces données, l’application permet au patient de construire son propre suivi, en sélectionnant les paramètres dont les courbes d’évolution pourront être visualisées ensemble, au sein d’un même graphique. Le patient peut également ajouter des mesures supplémentaires comme la température corporelle, des ressentis tels que la fatigue, l’essoufflement, les aspects des expectorations ou les douleurs. Il peut aussi ajouter des informations liées aux traitements (antibiotiques, médicaments, posologies, etc.). Une fonction d’extraction des données permet de créer un rapport que le patient peut partager avec son équipe soignante, pour l’informer à distance sur l’évolution de ses paramètres entre les différentes visites au sein du CRCM.
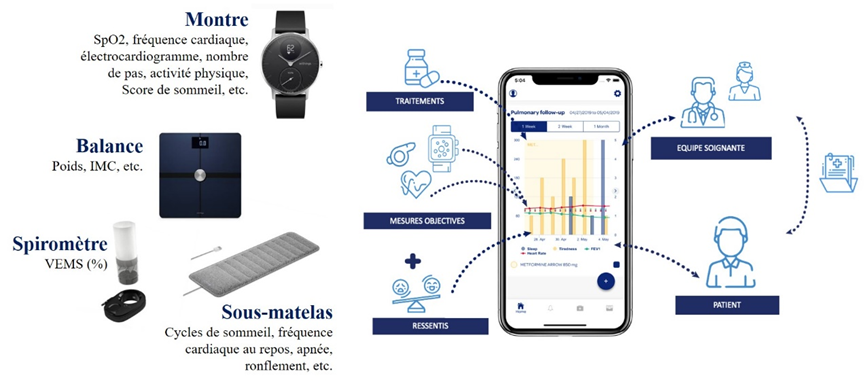
Figure 1. Composition et fonctionnement du dispositif numérique
L’analyse révèle plusieurs difficultés lors de l’introduction du dispositif dans la vie courante des patients. Son utilisation se caractérise par un nouveau faisceau de tâches censées intégrer le travail de surveillance de la maladie, via des pratiques de mesure et des formes d’attention qui, en règle générale, sont déjà particulièrement développées chez les personnes atteintes de mucoviscidose. Le dispositif s’insère ainsi au sein d’une « écologie des artefacts » (Mayère et al., 2012) bien fournie, voire même saturée, aux côtés d’autres outils de mesure utilisés par les patients (saturomètre, spiromètre, podomètre, etc.), et avec lesquels il entre en concurrence. À la différence de ces objets qui produisent séparément quelques données, l’objectif du dispositif numérique est de visualiser conjointement les évolutions de plusieurs paramètres sur un même graphe, et de dégager ainsi une tendance de fond pouvant être plus difficilement perceptible par les patients. Or, pour réaliser cette surveillance fine, le patient doit utiliser les objets connectés au quotidien, de manière assidue. L’analyse révèle à cet égard que les objets connectés n’ont jamais tous été utilisés conjointement, ou seulement rarement, durant de courtes périodes. Cela s’explique avant tout par la nécessité de sélectionner les objets et les données les plus pertinents à suivre selon les caractéristiques et l’expérience singulières de la maladie, qui varient pour chaque patient. Le dispositif a ainsi été pensé comme une boîte à outils composée d’une pluralité d’objets que chacun peut combiner selon ses propres besoins. Cependant, pour beaucoup de patients, les efforts à fournir pour construire ce suivi personnalisé ont pu constituer une difficulté supplémentaire dans le processus d’appropriation du dispositif dans son ensemble[4].
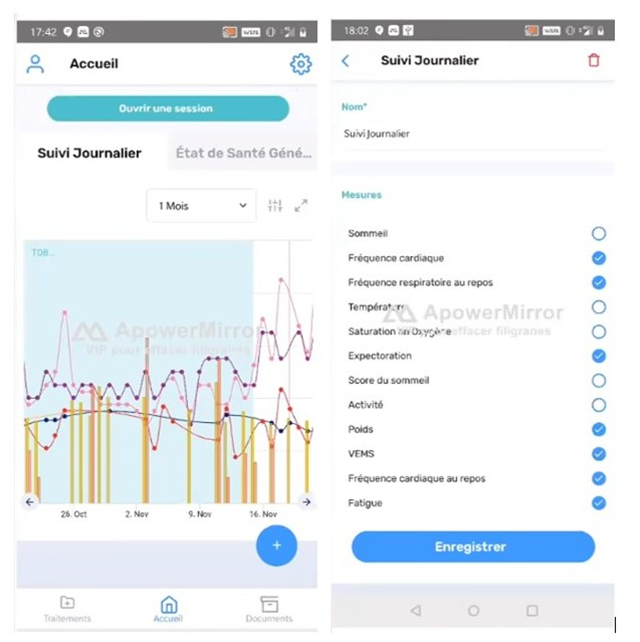
Figure 2. Paramétrage de visualisation des différentes catégories de mesure
Outre l’épreuve de la mise en place et du paramétrage, l’analyse met en lumière la grande diversité des usages du dispositif. Ainsi, les patients ne suivent pas tous les mêmes paramètres pour anticiper les exacerbations. Certains, par exemple, cherchent à surveiller la qualité du sommeil, qui peut s’amoindrir en raison de la toux, ou la baisse du VEMS et l’augmentation de la fréquence cardiaque mesurée au repos par le battement par minute (BPM), qui peuvent signaler un début d’infection :
« […] le rythme au repos sous infection est beaucoup plus élevé… parce que le corps lutte contre l’infection. Donc effectivement, je le constate sur mes rythmes au repos : au lieu de dormir à 60 BPM, je dors par exemple à 70. Donc s’il y a un doute sur le fait que je ne suis pas bien : "est-ce que c’est juste de la fatigue ou est-ce que je suis infecté ?", ça va être une information qui va être de valeur ». (Pierre, 25-30 ans, forme stable de la maladie, sous Kaftrio)
Si les patients sélectionnent les objets selon les pratiques d’autosurveillance développées au cours de leur trajectoire, ils les combinent aussi de manière singulière, selon les objectifs qu’ils se donnent dans la gestion quotidienne de la maladie. Lorsque les patients utilisent les mêmes objets, ils ne le font pas non plus pour les mêmes motifs. Certains privilégient, par exemple, la montre pour calculer le nombre de pas et suivre les performances sportives, alors que d’autres l’utilisent pour suivre la fréquence cardiaque au repos ou la saturation en oxygène. Parfois, les mêmes objets sont utilisés pour des objectifs symétriquement inverses : c’est le cas de la balance qui peut être utilisée soit pour perdre du poids et gagner en volume respiratoire, soit pour ne pas en perdre de trop, afin de préserver sa capacité à lutter contre une éventuelle infection.
Ainsi, les mêmes objets peuvent être intégrés de diverses manières dans l’autosurveillance des patients. Il en va de même pour la production et l’interprétation des différentes mesures : une même donnée n’a pas toujours la même signification et n’est pas non plus ressentie physiquement de la même façon : certains patients éprouvent bien des difficultés à respirer avec un pourcentage de VEMS que d’autres peuvent supporter plus aisément. Le dispositif s’intègre ainsi très diversement dans le cadre des expériences subjectives de la maladie. La temporalité des usages peut varier également dans l’expérience d’un seul et même patient, en fonction de l’évolution de son état de santé et, plus largement, des phases de la trajectoire de la maladie. Certains utilisent régulièrement plusieurs objets connectés simultanément, tandis que d’autres ne les mobiliseront que ponctuellement ou épisodiquement, lorsqu’ils constatent par exemple une dégradation de leur état de santé.
Les logiques de quantification de soi, entre « travail sur la maladie » et « travail sur la vie quotidienne avec la maladie »
Réalisée dans un contexte de bouleversement, la recherche permet cependant de décrire les usages du dispositif qui ne se développent pas là où ils étaient initialement attendus par les concepteurs et les soignants. C’est en effet en de très rares cas seulement que l’usage des objets connectés semble avoir permis de repérer les signes avant-coureurs d’une dégradation de l’état de santé. Néanmoins, l’analyse révèle plusieurs logiques de quantification qui se développent dans ce nouveau contexte thérapeutique, par exemple en cas d’aggravation de certains symptômes ou pour apprécier les effets positifs des cures et des traitements. D’autres usages plus quotidiens et durables se développent également, pour saisir des paramètres qui sont parfois moins directement liés à la maladie, notamment dans l’objectif d’instaurer une meilleure hygiène de vie et de réduire ainsi les risques d’exacerbation, de manière préventive.
De l’alerte à l’attention corporelle : des objets de quantification qui confirment les ressentis
Un des objectifs du dispositif numérique est d’enrichir les apprentissages que le patient est en mesure de développer à propos de lui-même et des manifestations de sa mucoviscidose, pour en améliorer la gestion quotidienne. Cette visée d’apprentissage trouve sa place chez certains patients particulièrement attachés à l’anticipation des manifestations de la maladie et à la limitation de leurs effets sur le déroulement de la vie quotidienne. Par exemple, Pierre qui sent généralement les dégradations arriver, essaie toujours d’anticiper et de programmer les perfusions d’antibiotiques à un moment jugé opportun. Cependant, malgré tous ses efforts et son ressenti, la cure par voie intraveineuse demeure parfois imprévisible. Il dit ainsi utiliser les objets connectés dans une logique d’optimisation, afin de se connaître encore mieux. Cette posture n’est cependant pas partagée par tous les patients qui ont développé une grande connaissance d’eux-mêmes et de leur corps, depuis leur plus jeune âge. Même si les ressentis ne suffisent pas toujours à repérer les premiers signes d’une exacerbation, les personnes vivant avec la mucoviscidose témoignent en effet, pour une grande part, d’une « attention corporelle » particulièrement aiguisée, souvent plus sensible que les objets connectés :
« […] quand je vais pas bien, parce que j’ai chopé un coup de froid ou que je suis fatigué, etc., je sais comment mon corps va me donner cette information. Je vais me sentir comme si j’avais une charge sur les épaules, je vais avoir mal dans les articulations, je vais avoir peut-être des maux de tête aussi pour me dire : "tiens, fais attention. Là, il y a peut-être un manque d’oxygène". Donc, je vais pas attendre, je vais tout de suite me mettre sous oxygène et puis je vais me mettre au repos. » (Claude, 50-55 ans, forme grave de la maladie, sous Kaftrio)
La majorité des patients interrogés ressentent ainsi physiquement divers signes avant-coureurs comme un essoufflement un peu plus marqué qu’à l’habitude, un début de toux ou une qualité de sommeil amoindrie. Pour ces patients, les usages du dispositif ne s’inscrivent donc pas dans une temporalité de crises. Les logiques de quantification qui se développent avec des objets souvent moins sensibles que les ressentis, alimentent au contraire une réflexivité qui repose sur l’articulation de plusieurs observations de moyen terme. Ainsi, pour certains patients, le dispositif permet d’apprécier les effets des traitements au cours d’une période donnée, pour saisir l’amélioration de l’état de santé. C’est le cas par exemple d’un patient qui, grâce au dispositif, constate une extension de la durée des périodes séparant les cures d’antibiotiques par voie intraveineuse, celles-ci passant de 4 à 6 semaines. Dans la plupart des cas, les patients procèdent à une comparaison entre les ressentis tirés de l’expérience corporelle et les mesures réalisées avec les objets connectés, souvent dans une logique de confirmation des premiers : « ça confirme que je ne me sens pas bien […] ça va plus confirmer des intuitions que j’avais déjà de toute façon […] ça remplace jamais l’impression » (Pierre, 25-30 ans, forme stable de la maladie, sous Kaftrio). Un autre patient évoque ses usages de la mesure et de l’estimation de la saturation, laquelle constitue pour lui un point de repère primordial pour distinguer bien-être et mal-être, qui est à la fois « ressenti » et mesuré :
« La saturation, c’est ultra important. Moi je suis capable de diagnostiquer ma saturation sans avoir à prendre un saturomètre, voilà ; parce que je me connais, je connais mon corps. Aujourd’hui, sans saturomètre, là, je suis à 92 % de saturation. Mais quand ça va pas et que je suis fatigué, je sais que je vais être à 88/89 et en général, le saturomètre, il me donne très souvent raison. » (Claude, 50-55 ans, forme grave de la maladie, sous Kaftrio)
C’est à la fois sa grande expérience en matière d’attention corporelle et son usage répété des outils de mesure qui expliquent le fait que ce patient soit capable de développer un ressenti extrêmement fin de la désaturation en oxygène et d’associer à son ressenti une valeur chiffrée.
Confrontation du « soi vécu » au « soi calculé » et repérage de nouveaux seuils sensoriels
Les activités de quantification s’accompagne de la confrontation de « l’expérience subjective » qui est tirée de l’attention corporelle, à « l’expérience calculée » par l’objet de mesure (Licoppe et al., 2013 ; Mathieu-Fritz & Guillot, 2017). Les patients sont très nombreux à affirmer la prééminence de la première, jugée beaucoup plus fine que les mesures : « […] si je vois que ma fréquence cardiaque accélère, ou alors, est très basse, et que ma saturation n’est pas super top, je vais déjà le ressentir avant même de regarder l’application de toute façon ». Cette primauté des ressentis repose, entre autres, sur le fait qu’ils relèvent de la singularité de chaque personne qui peut se sentir mal, même si les mesures paraissent a priori satisfaisantes sur le plan clinique. De plus, selon les périodes, les ressentis négatifs ne sont pas associées aux mêmes valeurs chiffrées ou aux mêmes seuils pour un même patient ; la maladie, les traitements et les ressentis pouvant évoluer au fil du temps : « […] pendant un temps, il fallait que je descende à 50 % [de capacité respiratoire] pour être pas bien […] à 60-70, je suis déjà plus bien, maintenant ». Ces variations de seuil récurrentes dans la trajectoire des patients, deviennent d’autant plus importantes avec l’arrivée du nouveau traitement, qui s’accompagne d’un bouleversement dans les ressentis. Une majorité de patients sous Kaftrio témoigne notamment du brouillage de certains repères perceptifs et sensoriels constitués au fil du temps, qui leur servaient auparavant à ressentir les prémices des dégradations de leur état de santé. Des décalages désormais se font jour par exemple entre ressenti et « expérience calculée » au CRCM, concernant la mesure de constantes comme le VEMS. En d’autres termes, le ressenti devient parfois trompeur :
« […] quand je suis à l’hôpital et que je fais le VEMS, des fois le premier coup, j’ai 25 %. Je me dis : "mais c’est pas possible !" J’ai l’impression d’en avoir… je suis tellement bien, j’ai une pêche d’enfer, c’est pas possible que j’ai 25, j’ai au moins 40 ». (Claude, 50-55 ans, forme grave de la maladie, sous Kaftrio)
Le système de perception sensorielle des patients paraît en partie bouleversé par le nouveau traitement, les signaux faibles de la maladie pouvant devenir moins perceptibles. Les objets connectés sont ainsi utilisés dans le cadre d’un « réétalonnage » des ressentis, pour identifier de nouveaux repères sensoriels et (ré)établir des seuils d’alerte. L’utilité du dispositif est ainsi réévaluée, à l’instar de Pierre qui, initialement très intéressé par le spiromètre, constate que toutes les mesures qu’il réalise sont identiques depuis plusieurs semaines, sa capacité respiratoire s’étant améliorée, puis stabilisée grâce au nouveau traitement. Pour lui, l’usage du spiromètre « a perdu de son sens » ; il peut redevenir utile durant de plus courtes périodes, lorsque les valeurs issues des mesures sont à la baisse, en raison par exemple d’un rhume favorisant la réapparition d’une toux. À l’inverse, alors que ce patient ne comptait pas faire usage de la balance connectée, celle-ci sera utilisée pour surveiller la prise de poids occasionnée par le nouveau traitement. Aussi, son usage de la montre connectée pour mesurer la fréquence cardiaque au repos lui permet désormais d’apprécier les effets liés au traitement avec le Kaftrio : « j’ai perdu 10 BPM la nuit ».
Même s’ils sont jugés moins précis que les outils de mesure utilisés à l’hôpital, les objets connectés sont considérés malgré tout comme fiables et utiles pour suivre des évolutions de la maladie, en particulier dans un contexte où les patients font face à des incertitudes associées à la prise du nouveau traitement. Ils permettent aux patients de multiplier les confrontations de leur ressenti corporel avec l’expérience calculée, pour le mettre progressivement en relation avec une mesure chiffrée : « j’essaie de me baser sur des chiffres : quand je vais bien, c’est comme ça, quand je vais pas bien, c’est comme ça ». Les mesures permettent ainsi de confirmer les ressentis, mais aussi, de manière moins prévisible par les patients ou les soignants, de les infirmer, les affiner et les réajuster pour que se constitue une nouvelle connaissance de soi, du corps et de la maladie sous Kaftrio. Dans ce contexte, les patients développent des logiques d’usages proches de celles du Quantified self (QS), où les objectifs de suivi de la maladie se voient reformulés et se traduisent par la visualisation de la progression et de la stabilisation de l’état de santé – et non plus celle de sa dégradation.
Le « Quantified self » dans la gestion de la maladie chronique, ou comment mesurer les effets du travail du patient ?
Les patients dont l’état de santé s’améliore et se stabilise avec le nouveau traitement, développent ainsi des logiques d’usage reposant sur les principes d’action du QS. Dans leurs discours, nous retrouvons tout d’abord la thématique de la transparence et de l’objectivation de soi, qui se fondent sur la régularité des mesures liées à l’activité physique et sportive, ainsi que sur l’attention prêtée à de nouveaux indicateurs jugés secondaires dans l’évaluation de l’état de santé, comme l’indice de masse corporelle (IMC), les différentes phases du sommeil ou le nombre de pas. Ces principes se traduisent par une forme de dévoilement et une prise de conscience conduisant à une (re)découverte de soi, c’est-à-dire un sentiment d’apprendre sur soi-même :
« […] on se rend compte qu’on a dormi seulement 4 heures […] j’avais pas ce genre de données, je savais pas, je dormais mal la nuit […] ça m’aide tous les jours à prendre conscience de tout ce que je fais dans la journée et des améliorations que je peux apporter » (Claude, 50-55 ans, forme grave de la maladie, sous Kaftrio)
Nous observons ici également les effets performatifs associés à la prise en compte des mesures chiffrées, qui font agir, réagir et réfléchir leurs utilisateurs :
« […] le spiro’ m’aide du coup entre deux rendez-vous médicaux, à voir aussi à la maison si j’ai baissé ou pas. Et le fait de voir si j’ai une grosse baisse, je me dis : "là, faut que je me bouge le cul, faut que j’aille courir", quoi. C’est que vraiment, il y a besoin de faire une activité physique [...] quand on a le chiffre sous les yeux, c’est un peu plus motivant, parce que si on tousse un petit peu ou qu’on n’est pas bien, on se dit : "bon, c’est passager". Si on voit que le VEMS, il commence à descendre, bon, là… on a les cartes en main, quoi, c’est à nous de faire quelque chose. » (Danielle, 25-30 ans, forme stable de la maladie, sous Kaftrio)
Outre les mesures, les outils assurent également une fonction de stockage, d’archivage, ainsi que de représentation des données produites. Le dispositif se présente ainsi comme un « artefact cognitif » (Norman, 2020), qui permet de détecter, d’interpréter l’état de santé, mais aussi d’agir (Datchary, 2005). Ces outils produisent des formes de quantification suivant une perspective diachronique, alimentant le sentiment d’une progression et favorisant l’émergence de pratiques caractérisées par la mise en place et le renforcement de boucles de rétroaction. Celles-ci témoignent non seulement de la réflexivité des utilisateurs (Licoppe et al., 2013), capables de faire retour sur leurs pratiques, leur corps et les manifestations typiques de « leur » mucoviscidose, mais également de la dimension performative des mesures qui les font (ré)agir, dans un souci d’optimisation de soi[5]. L’objectif est alors d’« aller encore plus loin » (Claude), en se fixant par exemple un poids à atteindre ou en poussant l’effort pendant l’activité physique : « C’est plus pour le dépassement de soi, c’est plus pour moi, de voir que je peux pousser plus loin » (Martine, 20-25 ans, forme stable de la maladie, sous Kaftrio). En filigrane apparaît ainsi le dernier principe du QS, le biohacking, qui consiste à augmenter son emprise sur ses performances physiques, son état de santé et son corps (Calvignac, 2021; Ruckenstein & Pantzar, 2019). En ce sens, les objets connectés viennent équiper les patients dans la gestion quotidienne de la maladie.
Si ces logiques de quantification traditionnelles du QS ne suivent pas une orientation médicale, elles permettent néanmoins de réaliser un auto-suivi de l’état de santé qui est toujours mis en lien plus ou moins directement avec le « travail du patient » désormais rendu visible et tangible par le dispositif :
« Si je faisais pas l’activité physique, je pense que la maladie prendrait beaucoup plus le pas sur moi. Donc le fait d’avoir une activité physique, ça me permet de garder la forme. Après, les données sont en plein rapport avec la muco. […] avec ma façon de vivre avec la maladie, etc. […] C’est pas des données qui vont être prises en compte dans un diagnostic médical. Par contre, ça va permettre de voir que grâce au traitement, grâce à l’activité physique, grâce à une alimentation saine et équilibrée, et ben... […] je peux faire beaucoup plus d’activités physiques qu’avant. […] c’est pour ça que c’est un outil précieux. (Claude, 50-55 ans, forme grave de la maladie, sous Kaftrio)
La logique d’optimisation de soi propre au QS prend donc, en l’occurrence, un sens différent. Les constantes et les paramètres permettent de mesurer les efforts réalisés pour mieux vivre avec la maladie et d’objectiver leurs effets sur la santé. Même si les patients bénéficiant du nouveau traitement mesurent davantage les progrès que les dégradations de leur état de santé, ces usages demeurent indéfectiblement liés à la pathologie. En identifiant les principes d’action du QS dans les logiques de quantification développées par les patients, l’analyse révèle ainsi une transformation des objectifs médicaux du dispositif en une conception particulière de la prise en charge et du travail du patient, qui se définit au-delà des activités de soin, à travers un travail sur soi plus large, plus exhaustif, englobant l’activité physique et l’état de santé général.
CONCLUSION
La prise en charge de la mucoviscidose se constitue à travers une série de caractéristiques touchant à la fois au profil des patients qui sont jeunes et relativement experts de leur maladie, à la relation de suivi marquée par une très forte proximité sociale avec les soignants, à l’intensité et à la densité du travail du patient autour de la gestion de la maladie, ainsi qu’aux objectifs thérapeutiques qui produisent parfois des incitations contradictoires dans l’autosurveillance, en dehors des milieux médicaux. Si l’enjeu est d’autonomiser les patients pour diminuer l’emprise de la maladie dans leur vie, l’analyse de l’intégration d’un nouveau dispositif d’autosurveillance connecté montre que cela se fait au prix d’un travail qui augmente le temps passé à se confronter à la pathologie. Réalisée dans un contexte d’amélioration de l’état de santé des patients liée au nouveau traitement, la recherche montre également que les usages de ce dispositif ne se sont pas développés suivant les attentes initiales, à savoir pour prévenir les exacerbations par une autosurveillance accrue de la pathologie. De nombreux enquêtés témoignent d’une perte d’intérêt pour les objets connectés dont le statut est jugé secondaire, non seulement parce que leurs usages arrivent dans un second temps, après les ressentis du patient qui sont plus précis et spécifiques à « sa » maladie, mais aussi parce que les valeurs chiffrées concernent des paramètres moins directement liées au suivi de la pathologie.
Les patients semblent néanmoins se saisir du dispositif lorsqu’ils sont confrontés, parfois avec leur équipe soignante, à de nouvelles formes d’incertitude liées à leur état de santé. L’analyse révèle plusieurs logiques de quantification de soi qui sont développées suivant la typologie et la sévérité de leur pathologie. Certains patients utilisent ainsi les objets connectés de façon ponctuelle ou épisodique, à l’occasion des périodes de dégradation. Le dispositif permet alors de mesurer les effets d’un traitement, comme une cure d’antibiotiques, ou du Kaftrio qui, dès les premières prises, bouscule les repères sensoriels des patients. D’autres réalisent, à l’inverse, un suivi plus régulier pour objectiver les évolutions positives de leur état de santé. Les logiques de quantification se rapprochent ici des pratiques plus traditionnelles de QS, inscrites dans le cadre d’une activité sportive et, plus largement, de la recherche d’une meilleure hygiène de vie. Pour ces patients, il ne s’agit plus tant d’anticiper les exacerbations, que de constater les progressions et un mieux-être liés aux effets conjugués des activités physiques et sportives et du nouveau traitement. Ainsi, le dispositif semble agir davantage sur le « travail sur la vie quotidienne avec la maladie » (hygiène de vie, activités sportives, repos, etc.) et sur le « travail biographique » comprenant la (re)définition de soi et de sa vie (future) avec la pathologie (Bury, 1982 ; Corbin & Strauss, 1987), plutôt que sur le « travail sur la maladie », périmètre initialement visé par les concepteurs. Ce suivi proche des pratiques de QS est ainsi toujours mis en relation avec la pathologie chronique et son contexte, qui demeure marqué par des incertitudes, car les personnes ayant pu bénéficier des avancées liées au Kaftrio ne sont pas pour autant guéries, et ne sont pas tout à fait à l’abri d’éventuelles dégradations de leur état de santé.
RÉFÉRENCES BIBLIOGRAPHIQUES
Anderson, R. M., & Funnell, M. M. (2010). Patient Empowerment : Myths and Misconceptions. Patient education and counseling, 79(3), 277‑282. https://doi.org/10.1016/j.pec.2009.07.025
Bach, M.-A. (1995). La sclérose en plaques entre philanthropie et entraide : L’unité introuvable. Sciences Sociales et Santé, 13(4), 5‑38. https://doi.org/10.3406/sosan.1995.1340
Baszanger, I. (1986). Les maladies chroniques et leur ordre négocié. Revue française de sociologie, 27(1), 3‑27. https://doi.org/10.2307/3321642
Bell, S. C., Mall, M. A., Gutierrez, H., Macek, M., Madge, S., Davies, J. C., Burgel, P.-R., Tullis, E., Castaños, C., Castellani, C., Byrnes, C. A., Cathcart, F., Chotirmall, S. H., Cosgriff, R., Eichler, I., Fajac, I., Goss, C. H., Drevinek, P., Farrell, P. M., … Ratjen, F. (2020). The future of cystic fibrosis care : A global perspective. The Lancet Respiratory Medicine, 8(1), 65‑124. https://doi.org/10.1016/S2213-2600(19)30337-6
Bruni, A., & Rizzi, C. (2013). Looking for data in diabetes healthcare : Patient 2.0 and the re-engineering of clinical encounters. Science & Technology Studies, 26(1), 29‑43.
Bury, M. (1982). Chronic illness as biographical disruption. Sociology of Health & Illness, 4(2), 167‑182.
Calvignac, C. (2021). Traductions sociotechniques des principes axiologiques du quantified self. Analyse d’un corpus de brevets US dédiés à la mesure et à la gestion du sommeil. Réseaux, 228(4), 131‑169. https://doi.org/10.3917/res.228.0131
Carricaburu, D. (2000). L’hémophilie au risque de la médecine. Economica.
Carricaburu, D., & Ménoret, M. (2004). Chapitre 6—Maladies chroniques et normalisation. In Sociologie de la santé (p. 91‑106). Armand Colin. https://doi.org/10.3917/arco.carri.2004.01.0091
Castro, E. M., Van Regenmortel, T., Vanhaecht, K., Sermeus, W., & Van Hecke, A. (2016). Patient empowerment, patient participation and patient-centeredness in hospital care : A concept analysis based on a literature review. Patient Education and Counseling, 99(12), 1923‑1939. https://doi.org/10.1016/j.pec.2016.07.026
Corbin, J., & Strauss, A. (1985). Managing chronic illness at home : Three lines of work. Qualitative Sociology, 8(3), 224‑247.
Corbin, J., & Strauss, A. (1987). Accompaniments of chronic illness : Changes in body, self, biography, and biographical time. Research in the Sociology of Health Care, 6, 249‑281.
Dagiral, É., Licoppe, C., Martin, O., & Pharabod, A. S. (2019). Le Quantified Self en question(s). Une revue de littérature des travaux de sciences sociales consacrés à l’auto-mesure des individus. Reseaux, 4(216), 17‑54.
Datchary, C. (2005). Se disperser avec les TIC, une nouvelle compétence?
David, V., Iguenane, J., & Ravilly, S. (2007). L’éducation thérapeutique dans la mucoviscidose : Quelles compétences pour le patient ? Présentation du référentiel des compétences adulte-enfant. Revue des Maladies Respiratoires, 24(1), 57‑62. https://doi.org/10.1016/S0761-8425(07)91012-8
Ferez, S., Silvestri, L., & Issanchou, D. (2023). L’ombre du handicap : Parcours scolaires et professionnalisation avec la mucoviscidose. PUG.
Frattini, M.-O., Houzard Rocamora, S., & Sermet-Gaudelus, I. (2009). La mucoviscidose : Ajustements entre pratiques professionnelles et travail des malades et de leurs proches. Santé, Société et Solidarité, 8(2), 111‑117. https://doi.org/10.3406/oss.2009.1366
Jamieson, N., Fitzgerald, D., Singh-Grewal, D., Hanson, C. S., Craig, J. C., & Tong, A. (2014). Children’s experiences of cystic fibrosis : A systematic review of qualitative studies. Pediatrics, 133(6), e1683-1697. https://doi.org/10.1542/peds.2014-0009
Kerem, E., Conway, S., Elborn, S., & Heijerman, H. (2005). Standards of care for patients with cystic fibrosis : A European consensus. Journal of Cystic Fibrosis, 4(1), 7‑26. https://doi.org/10.1016/j.jcf.2004.12.002
Langeard, C., & Minguet, G. (2018). Généalogie des bonnes pratiques d’hygiène : Déclinaisons locales et travail d’accord dans le cas de la mucoviscidose. Sciences Sociales et Santé, 36(1). https://doi.org/10.1684/sss.2018.0103
Langeard, C., Minguet, G., Guéganton, L., Cam, P., Faquet, C., Lombrail, P., & Rault, G. (2011). L’expérience professionnelle du médecin hospitalier à l’épreuve du dépistage : Le cas de l’annonce du diagnostic de la mucoviscidose. Revue française des affaires sociales, 2‑3, 80‑102. https://doi.org/10.3917/rfas.112.0080
Licoppe, C., Draetta, L., & Delanoë, A. (2013). Des « smart grids » au « quantified self ». Technologies réflexives et gouvernement par les traces, une étude de cas sur la consommation électrique en milieu domestique. Intellectica, 59(1), 267‑290.
Lupton, D. (2016). The Quantified Self. John Wiley & Sons.
Mathieu-Fritz, A., & Guillot, C. (2017). Les dispositifs d’autosurveillance du diabète et les transformations du « travail du patient ». Revue d’anthropologie des connaissances, 11(4), 641‑675.
May, C. R., Eton, D. T., Boehmer, K., Gallacher, K., Hunt, K., MacDonald, S., Mair, F. S., May, C. M., Montori, V. M., Richardson, A., Rogers, A. E., & Shippee, N. (2014). Rethinking the patient : Using Burden of Treatment Theory to understand the changing dynamics of illness. BMC Health Services Research, 14(1), 281. https://doi.org/10.1186/1472-6963-14-281
Mayère, A., Bazet, I., & Roux, A. (2012). « Zéro papier » et « pense-bêtes » à l’aune de l’informatisation du dossier de soins. Revue d’anthropologie des connaissances, 6(1), Article 1. https://doi.org/10.3917/rac.015.0154
Ménoret, M. (2015). La prescription d’autonomie en médecine. Anthropologie & Santé. Revue internationale francophone d’anthropologie de la santé, 10, Article 10. https://doi.org/10.4000/anthropologiesante.1665
Mol, A. (2009). Ce que soigner veut dire : Repenser le libre choix du patient. Mines ParisTech, Presses des mines.
Moretti, V., & Morsello, B. (2017). Self–management and Type 1 Diabetes. How Technology Redefines Illness. TECNOSCIENZA: Italian Journal of Science & Technology Studies, 8(1), 51‑72.
Norman, D. A. (2020). Les artefacts cognitifs. In B. Conein, N. Dodier, & L. Thévenot (Éds.), Les objets dans l’action : De la maison au laboratoire (p. 15‑34). Éditions de l’École des hautes études en sciences sociales. https://doi.org/10.4000/books.editionsehess.9870
Pichonnaz, D. (2024). Travailler avec la mucoviscidose. Capitaux familiaux et socialisation par la maladie. In A. Gonnet, L. Lima, P. Carloni, L. Le Gros, M. Matus, & C. Tuchszirer (Eds.), L’accompagnement des transitions professionnelles : Un monde en soi ? Institutions, métiers, expériences (Éditions Teseo).
Rault, G., Pougheon, D., Moisdon, J.-C., Pépin, M., Kletz, F., Bellon, G., Durieu, I., & Lombrail, P. (2015). Analyse de la prise en charge hospitalière ambulatoire de la mucoviscidose. Santé Publique, 27(3), 363‑372. https://doi.org/10.3917/spub.153.0363
Raveneau, G. (2020). Proximité et mise à distance du corps souffrant dans le récit de la maladie d’adolescents. Corps, 18(1), 213‑234. https://doi.org/10.3917/corp1.018.0213
Ruckenstein, M., & Pantzar, M. (2019). Par-delà le Quantified Self. Exploration thématique d’un paradigme dataïste. Réseaux, 216(4), 55‑81. https://doi.org/10.3917/res.216.0055
Star, S. L. (1991). The sociology of the invisible : The primacy of work in the writings of Anselm Strauss. In D. Maines (Éd.), Social organization and social process : Essays in honor of Anselm Strauss (p. 265‑283). Aldine de Gruyter.
Star, S. L., & Strauss, A. (1999). Layers of silence, arenas of voice : The ecology of visible and invisible work. Computer Supported Cooperative Work (CSCW), 8(1), 9‑30.
Strauss, A. L. (1975). Chronic illness and the quality of life. Mosby.
Strauss, A. L. (1978). Negotiations : Varieties, contexts, processes and social order. Jossey-Bass Inc.
Strauss, A. L. (1985). Social organization of medical work. University of Chicago Press.
Strauss, A. L. (1992). La trame de la négociation : Sociologie qualitative et interactionnisme. Harmattan.
Strauss, A. L., Fagerhaugh, S., Suczek, B., & Wiener, C. (1981). Patients’ work in the technologized hospital. Nursing Outlook, 29(7), 404‑412.
Strauss, A. L., Fagerhaugh, S., Suczek, B., & Wiener, C. (1982). The work of hospitalized patients. Social Science & Medicine, 16(9), 977‑986. https://doi.org/10.1016/0277-9536(82)90366-5
Travert, G., Sermet-Gaudelus, I., Edelman, A., & Fiant, D. (2024). La fatalité de la mucoviscidose sera-t-elle vaincue ? Histoire et succès. l’Harmattan.
Trupia, D. V., Mathieu-Fritz, A., & Duong, T. A. (2021). The Sociological Perspective of Users’ Invisible Work : A Qualitative Research Framework for Studying Digital Health Innovations Integration. Journal of Medical Internet Research, 23(11), e25159. https://doi.org/10.2196/25159
NOTES
[1] Intitulé « Accompagnement à l’autonomie en santé des patients adultes atteints de mucoviscidose à l’aide des nouvelles technologies », le projet de recherche a été porté et réalisé par le laboratoire LATTS (UMR - CNRS 8134), en partenariat avec le CRCM de l’hôpital Foch et la société Pheal, avec le soutien financier de l’Association Grégory Lemarchal et l’autorisation du Comité d’Éthique de la Recherche de l’hôpital Foch. Il a été complété par une enquête réalisée auprès des professionnels de santé libéraux, en particulier des kinésithérapeutes (n=10) et des psychologues (n=10), avec le soutien de la Fondation Maladies Rares. Nous tenons à remercier très chaleureusement Antoine Bertrand qui a joué un rôle essentiel dans la mise en place et la réalisation de ces études. Nous remercions également le Dr Dominique Grenet et son équipe pour leur engagement tout au long de la recherche, malgré le contexte pandémique, ainsi que tous les patients qui ont accepté d’y contribuer. L’ensemble des propos cités est anonymisé.
[2] Le recrutement des patients a été assuré principalement par l’équipe soignante du CRCM de l’hôpital Foch, selon des critères de diversification permettant de couvrir globalement la variété des profils des patients atteints de mucoviscidose, allant des personnes très peu touchées par les manifestations de la maladie à celles plus sérieusement atteintes. Le panel est composé de 4 femmes et 9 hommes, des individus principalement jeunes (9 ont entre 20 et 30 ans) ; toutefois, 2 personnes ont entre 30 et 40 ans, et 2 autres entre 40 et 50 ans. La majorité de ces patients se situe ainsi à un moment charnière de leur existence, marqué par un ensemble de changements qui s’opèrent traditionnellement lorsque démarre la vie adulte (autonomisation, déménagement, mise en ménage, etc.). Parmi ces jeunes patients, 4 habitent chez leurs parents, tandis qu’au moins 3 ont mentionné avoir déménagé au cours de l’étude. Aussi, 4 patients sont encore étudiants et 3 autres occupent leur premier emploi. Parmi les patients adultes, on retrouve également 4 jeunes actifs, 1 patient sans emploi pour des raisons liées à la maladie et 2 autres patients plus âgés, qui sont plus avancés dans leur carrière professionnelle.
[3] Au sein de notre échantillon, 11 participants sur 13 ont bénéficié du nouveau traitement.
[4] Les patients se sont notamment heurtés à des problèmes pratiques dans le cadre de la mise en route du dispositif qui, encore en phase expérimentale, nécessitait d’importants efforts lors de la première installation et synchronisation des objets. Récupérant les objets connectés dans leur emballage d’origine au sein de leur CRCM, les patients ont en effet découvert le dispositif par eux-mêmes, à leur domicile. Après avoir connecté chaque objet selon les différents modes d’emploi, les patients étaient invités à suivre les étapes détaillées par les concepteurs du dispositif, pour installer et paramétrer les applications mobiles permettant de centraliser, synchroniser et visualiser les données collectées. Ces différentes étapes n’ont pas pu faire l’objet d’un accompagnement ni être observées dans le cadre de la recherche.
[5] Précisons que les logiques d’usage proches du QS, dans la perspective de saisir des évolutions positives de l’état de santé avec la pathologie chronique, sont aussi observables chez des patients qui ne sont pas éligibles au Kaftrio.

 Télécharger l'article
Télécharger l'article

 Contacter l'auteur
Contacter l'auteur
 Lire la suite
Lire la suite